Asthma bronchiale in den Griff bekommen: eine Fallstudie
Patient case study:
Die Fotos und der Name sind nicht die eines echten Patienten und dienen nur der Veranschaulichung.
„Ich atme ein und aus, und schließe meine Augen um all Sinneseindrücke warzunehmen. Das Zwitschern der Vögel in der Ferne und die Wärme der Sonne auf meinem Gesicht, während sie über dem Horizont aufgeht. So stelle ich mir vor, wie es sich auf dem Berggipfel anfühlen würde, den ich von meinem Küchenfenster aus sehe. Jeden Monat erklimmt meint örtlicher Wanderverein diesen Berg und erzählt mir, wie atemberaubend es ist, den Sonnenaufgang von dort oben zu erleben. Ich hätte nie gedacht, dass ich das einmal erleben würde. Aber dieses Jahr ist anders.“
Isabel, Asthmapatientin
„Ein beeindruckender Aufstieg“ erzählt die Geschichte von Isabel, einer 60-Jahre alten Frau, die schon immer davon geträumt hat, gemeinsam mit anderen Wanderern einen Berg mit spektakulärer Aussicht zu erklimmen, der bei Einheimischen und Touristen gleichermaßen beliebt ist. Jeden Tag schaut sie beim Abwasch auf den Berg und stellt sich vor, wie es wäre, endlich auf dem höchsten Punkt zu stehen und goldene Sonnenstrahlen über dem Tal und ihrem Haus zu sehen. Aber für Isabel sind lange Wanderungen anstrengend, und sie ist schon bei kleineren Anstrengungen außer Atem. Könnte die Antwort in einer Änderung ihres Asthma-Managements liegen?
Diese Geschichte wurde von einem Patientenfall übernommen, der von Dr. Abel Pallarés Sanmartín, Leiter der Abteilung für Pneumologie, Universitätskrankenhaus von Ourense, Spanien, behandelt wurde. Dies ist nur ein beispielhafter Patientenfall, der zur Veranschaulichung dient. Behandlungseffekte und Erfahrungen können bei jedem Patienten unterschiedlich sein. Die jeweilige Behandlungsmethode muss vom behandelnden Arzt von Fall zu Fall gewählt werden.
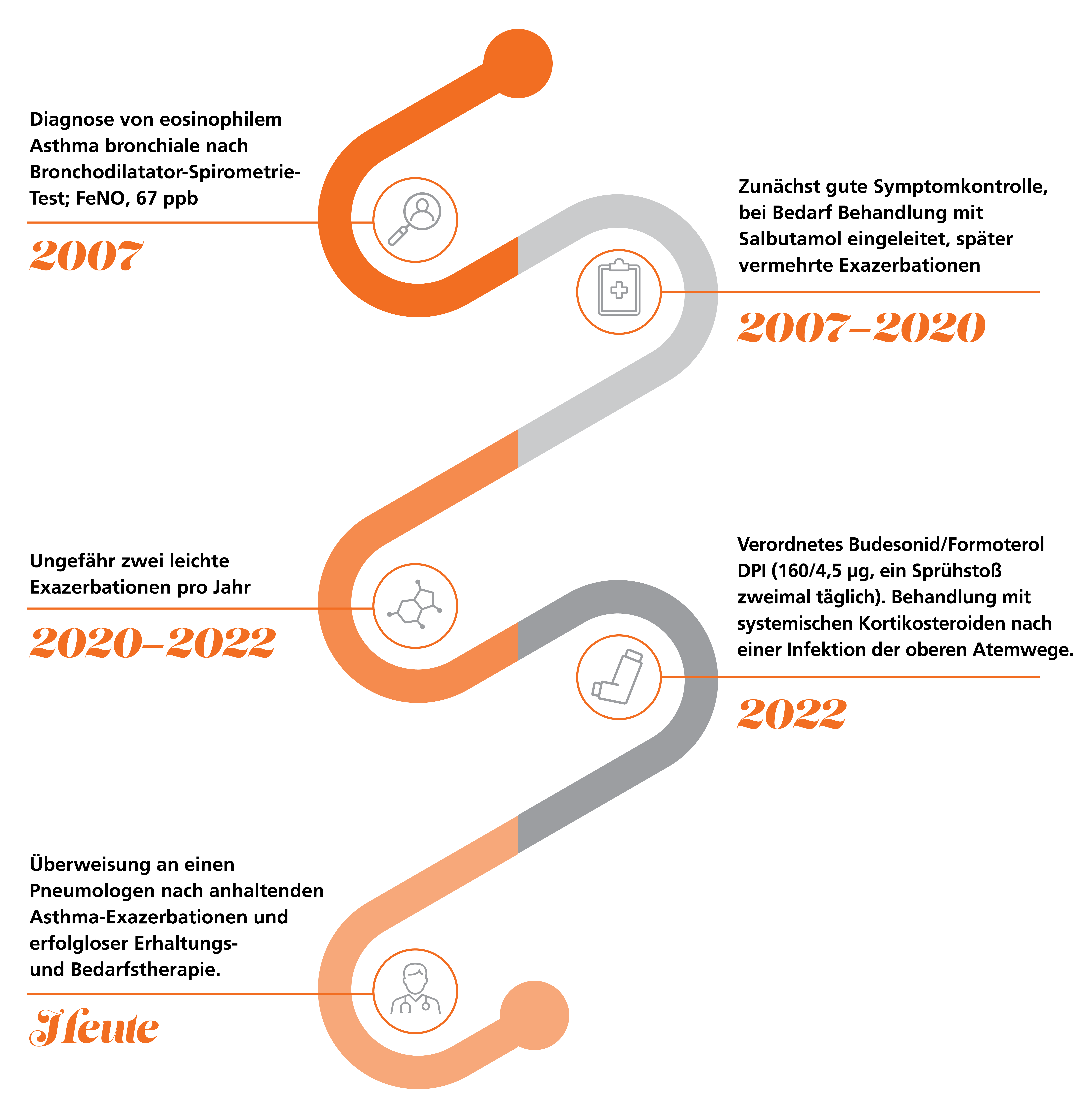
Isabels bisheriger Weg
Isabel bemerkte vor 15 Jahren ihre Symptome zum ersten Mal. Isabel war daran gewöhnt, den ganzen Tag auf den Beinen zu sein, aber ihr Arbeitspensum fiel ihr zunehmend schwerer als zuvor. Sie war oft bei den kleinsten Aufgaben außer Atem, wie z. B. beim Treppensteigen.
Sie vereinbarte einen Termin bei ihrer Hausärztin und nach einer vollständigen diagnostischen Abklärung wurde ihr mitgeteilt, dass sie an eosinophilem Asthma bronchiale litt.
Mit einem festen Behandlungsplan konnte Isabel ihre Symptome über ein Jahrzehnt lang in den Griff bekommen, ihr Reinigungsgeschäft weiterführen und versuchen, Kraft aufzubauen, um den schwierigen Gipfel zu bezwingen.
Doch vor zwei Jahren begannen die Krankheitsbeschwerden zuzunehmen. Sie versuchte, ihren Behandlungsplan so gut wie möglich zu befolgen, aber ihre Symptome eskalierten, und bald hatte sie etwa zweimal im Jahr leichte Exazerbationen.
Ihr Arzt versuchte, mit der Verordnung von Budesonid/Formoterol DPI (160/4,5 µg, ein Sprühstoß zweimal täglich) ihr Asthma in den Griff zu bekommen, und Isabel hoffte, dass ihre Symptome bald abklingen würden. Nach sechs Monaten erkrankte sie jedoch an einer Infektion der oberen Atemwege und wurde mit Kortikosteroiden behandelt. Einen Monat später erlitt Isabel weitere Exazerbationen und erhielt eine Erhaltungs- und Bedarfstherapie.
Trotz der Behandlung benötigte Isabel eine Notfallmedikation mittels Inhalation und systemischen Kortikosteroiden und wurde an einen Pneumologen überwiesen.

Abkürzungen
BID, zweimal täglich; DPI, Trockenpulverinhalator; FeNO, Fraktioniertes exhaliertes Stickstoffmonoxid; ppb, Teile pro Milliarde.
Klinische Präsentation
Auf Anraten ihrer Hausärztin ging Isabel zu einem Pneumologen. Sie berichtete von starken Angstzuständen, und ihr Asthma war nur noch schlecht unter Kontrolle. Dies spiegelte sich in ihrem ACT-Wert von 13 wider, bei dem sie nachmittags und nachts stärkere Symptome hatte. Obwohl Isabel ihren Erhaltungs-Inhalator 6–7 Mal pro Tag benutzte, hatte sie innerhalb von 12 Monaten drei Exazerbationen und erhielt 450 mg orale Kortikosteroide.
Obwohl Isabel eine basale Sauerstoffsättigung von 97% aufwies, zeigte eine Lungenauskultation endrespiratorisches Keuchen. Rhinitis, Sinusitis, gastroösophagealer Reflux, Polypen, Septumdeviation und nächtliche Apnoe wurden ausgeschlossen, zusammen mit der Bestätigung, dass sie keine allergischen Sensibilisierungen hatte. Nachdem ihr Arzt ihre Inhalationspraxis mithilfe des In-Check Dials überprüft hatte, stellte er fest, dass sie nicht in der Lage war, die Inhalation erfolgreich durchzuführen.
Bei Isabel wurde ein spät einsetzendes schweres persistierendes eosinophiles Asthma ohne allergische Sensibilisierung und mit schlechter Kontrolle diagnostiziert.
Welche anderen Komorbiditäten gibt es in Isabels Krankengeschichte?
 | Perenniale Rhinitis |
 | Angstzustände, behandelt mit Lorazepam |
- BMI: 22 kg/m2

- Eosinophilenzahl im Blut: 450 Zellen/µl
- Pricktest: Keine allergische Sensibilisierung

- ACT-Score: 13;
Wünschenswerter Bereich ≥201* - HADS Test Score: 15;
Wünschenswerter Bereich ≤72**
- FEV1: 1650 mL (77%);
Nach dem Bronchodilatator: +280 ml (+13%);
Wünschenswerter Bereich ≥70%3† - FVC: 2480 mL (93%);
Wünschenswerter Bereich ≥80%3† - FEV1/FVC: 66%;
Wünschenswerter Bereich ≥70%3 - FeNO: 46 ppb;
Wünschenswerter Bereich <25 ppb5‡

- Röntgenaufnahme des Brustkorbs:
Keine akuten pleuroparenchymalen Anomalien
*≥20 bedeutet kontrolliertes Asthma, 16–19 bedeutet teilweise kontrolliert, < 16 bedeutet unkontrolliert.1
**Ein Wert von 7 oder weniger gilt als normal, während 8–10 auf grenzwertige/leichte Fälle hindeuten und 11–21 auffällig sind, was auf Angstzustände und/oder Depression hindeutet.2
†>70% pred bedeutet leichte Atemwegsobstruktion, 60–69 % pred bedeutet mäßig, 50–59 % pred bedeutet mäßig schwer, 35–49 % pred bedeutet schwer, < 35 % pred bedeutet sehr schwer.4
‡25-50 ppb gilt als intermediär und >50 ppb ist hoch, was auf eine Entzündung der Atemwege hinweist.5
Abkürzungen und Referenzen
ACT, Asthmakontrolltest; BMI, body mass index; FeNO, Fraktioniertes exhaliertes Stickstoffmonoxid; FEV1, forciertes exspiratorisches Volumen in einer Sekunde; FVC, forcierte Vitalkapazität; HADS, Krankenhausangst- und Depressionsskala; ppb, Teile pro Milliarde.
1. Soler X, et al. Allerg Clin Immunol Pract. 2018;6(1):151–158.
2. Rishi P, et al. Indian J Ophalmol. 2017;65(11):1203–1208.
3. Barreiro TJ and Perillo I. Am Fam Physician. 2004;69(5):1107–1114.
4. Quanjer PH, et al. Eur Respir J. 2014;43:505–512.
5. Miskoff JA et al. Cureus. 2019;11(6):e4864.

Behandlungsentscheidungen
Ohne Kontrolle über ihre Symptome schien Isabels Traum von der Eroberung des Berges unerreichbar. Ihr Pneumologe entschied, dass eine Änderung der therapeutischen Strategie unerlässlich sei.
Nachdem festgestellt wurde, dass die Inhalationstechnik von Isabel unzureichend war und unter Berücksichtigung ihrer verminderten Inspirationskapazität wurde die Behandlung auf eine hohe Dosis Kortikosteroide erhöht und von einem DPI auf einen pMDI umgestellt. Angesichts der mangelnden Kontrolle der Symptome, die Isabel mit ihrem Inhalator als Erhaltungs- und Entlastungstherapie (MART) erreicht hatte,1 entschied sich ihr Arzt, flutiform® (Fluticasonpropionat/Formoterol)- 250/10 µg, 2 Sprühstöße zweimal täglich, zusammen mit einem SABA-Reliever, zu verabreichen.
Isabel erhielt außerdem eine Anleitung, wie sie ihren Inhalator richtig anwenden sollte. Durch die bessere Kontrolle ihres Asthmas konnte Isabel eine potenzielle Angstquelle beseitigen2 und die Dinge genießen, nach denen sie sich so sehr sehnte.
Abkürzungen und Referenzen
BID, zweimal täglich; DPI, Trockenpulverinhalator; pMDI, druckgasbetriebener Dose-Inhalator; SABA, kurzwirkender ß2 Agonist.
1. Chapman KR, et al. Thorax. 2010 Aug;65(8):747-52.
2. Del Giacco SR, et al. Respiratory Medicine 2016.120:44-53.
Warum flutiform® (Fluticasonpropionat/ Formoterol) pMDI?
Der flutiform® pMDI wurde gewählt, um Isabels unkontrolliertes Asthma zu behandeln, weil es damit

zu weniger schweren Asthma-Exazerbationen kommt1–5
- Mit flutiform® pMDI kommt es zu weniger schweren Asthma-Exazerbationen in RCT-1und RWE-Studien im Vergleich zu anderen ICS/LABA-Kombinationen.1–4
- Eine im Jahr 2022 durchgeführte Metaanalyse zeigte, dass flutiform® pMDI Risiko schwerer Asthma-Exazerbationen reduziert und die Wahrscheinlichkeit erhöht, bei Asthmapatienten unter realen Bedingungen eine Asthmakontrolle zu erreichen.5
Bleiben Sie auf dem Laufenden über die Behandlung mit flutiform® pMDI bei Asthma-Exazerbationen.

signifikante Verbesserungen bei der Asthmakontrolle in der Praxis kommt2–4,6
- Beobachtungsstudien zeigen, dass die Behandlung mit flutiform® pMDI den Anteil der Patienten mit gut kontrolliertem Asthma gegenüber Baseline erhöht, der sich nach 12 Monaten Behandlung mit flutiform® pMDI mehr als verdoppelt.2,3
- Ein signifikant höherer Anteil der Patienten erreichte kontrolliertes Asthma nach der Umstellung von Fluticasonpropionat/Salmeterol auf. flutiform® pMDI6
Erfahren Sie mehr über die Praxis-Evidenz für eine verbesserte Asthmakontrolle mit flutiform® pMDI.

eine Persistenz und Therapietreue gibt4
- Patienten, die flutiform® pMDI erhielten, wurden im Vergleich zu anderen ICS/LABA-Kombinationen mit einer höheren Therapietreue in Verbindung gebracht.4
Entdecken Sie die Videoplattform zum Asthma-Management mit flutiform® pMDI.
Sicherheitsprofil von flutiform® pMDI anzeigen.
- Die Sicherheit und Verträglichkeit von flutiform® pMDI wurde während der klinischen Entwicklung gut untersucht und unerwünschte Ereignisse sind in der Fachinformation von flutiform® pMDI angegeben..7
Abkürzungen
ICS, inhalatives Kortikosteroid; LABA, langwirkender ß2 Agonist; pMDI, Druck-Dosier-Inhalator RCT, randomisierte kontrollierte Studie; RWE, Real-World Evidenz.
1. Papi A, et al. J Aerosol Med Pulm Drug Deliv. 2016;29:346–361.
2. Schmidt O, et al. Respir Med. 2017;131:166–174.
3. Backer V, et al. Ther Adv Respir Dis. 2018;12:1–16.
4. Sicras-Mainar A, et al. BMJ Open. 2022;12(4):e053964.
5. Papi A, et al. Eur Clin Resp J. 2023;10(2174642):1–10.
6. Usmani O S, et al. J Allerg Clin Immunol Prac. 2017;5(5):1378–87.
7. Fachinformation flutiform® pMDI, Stand Mai 2021.
Das Ergebnis bei Isabel
Es ist jetzt ein Jahr her, dass Isabel ihren Termin beim Pneumologen hatte, und sie hat das Gefühl, dass sich ihr Asthma-Management verbessert hat. Ihre Inhalationstechnik ist viel wirksamer und ihre verbesserten Spirometrie- und FeNO-Ergebnisse wurden aufrechterhalten. Bei minimalem Bedarf an Notfallmedikation hatte Isabel keine weitere Exazerbation und benötigt keine oralen Kortikosteroide mehr.
Und Isabel kann sich jetzt ihren Wanderfreunden anschließen und sich auf den Weg nach oben machen, um den Sonnenaufgang auf dem Gipfel zu erleben. Nach Jahren des Wartens kann Isabel endlich den anspruchsvollen Aufstieg wagen.
Seit Beginn der Behandlung mit flutiform® pMDI, ist Isabel in der Lage, ihre Symptome unter Kontrolle zu bringen und ihr Leben wieder selbst in die Hand zu nehmen. Mit einem ACT-Score von 23 hat sie erhebliche Verbesserungen bei ihren Symptomen bemerkt, und ihre verbesserte Lungenfunktion und FeNO-Spiegel wurden aufrechterhalten. Isabel fühlt sich selbstbewusster und bestärkt, und ihre Angstzustände1 sind auf dem HADS-Fragebogen auf einen Wert von 9 (grenzwertig/leicht) gesunken. Vor allem hat sie keine weiteren Exazerbationen mehr gehabt, was eine Verbesserung der Behandlung darstellt, da sie keine Notfallmedikamente und oralen Kortikosteroide mehr benötigt.
Vor Beginn der Behandlung mit flutiform® pMDI:
Image

|
|
Image
|
|
Nach Beginn der Behandlung mit flutiform® pMDI:
Image

|
|
Image

|
|
*≥20 bedeutet kontrolliertes Asthma, 16–19 bedeutet teilweise kontrolliert, <16 bedeutet unkontrolliert.2
**Ein Wert von 7 oder weniger gilt als normal, während 8–10 auf grenzwertige/leichte Fälle hindeuten und 11–21 auffällig sind, was auf Angstzustände und/oder Depression hindeutet.3
†>70 % pred bedeutet leichte Atemwegsobstruktion, 60–69% pred bedeutet mäßig, 50–59% pred bedeutet mäßig schwer, 35–49% pred bedeutet schwer, <35% pred bedeutet sehr schwer.5
‡25–50 ppb gilt als mäßig und >50 ppb gilt als hoch, was auf eine Entzündung der Atemwege hinweist.6
Abbreviations
ACT, Asthmakontrolltest; FeNO, Fraktioniertes exhaliertes Stickstoffmonoxid; FEV1, forciertes exspiratorisches Volumen in einer Sekunde; FVC, forcierte Vitalkapazität; HADS, Krankenhausangst-und Depressionsskala; pMDI, ruckgasbetriebener Dosier-Inhalator; ppb, Teile pro Milliarde.
1. Del Giacco SR, et al. Respiratory Medicine 2016.120:44-53
2. Soler X, et al. Allerg Clin Immunol Pract. 2018;6(1):151–158.
3. Rishi P, et al. Indian J Ophalmol. 2017;65(11):1203–1208.
4. Barreiro TJ and Perillo I. Am Fam Physician. 2004;69(5):1107–1114.
5. Quanjer PH, et al. Eur Respir J. 2014;43:505–512.
6. Miskoff JA et al. Eur Respir J. 2019;11(6):e4864.
Wichtigste Erkenntnisse
Ein optimales Asthma-Management könnte das Leben von Patienten wie Isabel verbessern.
Wie können Sie Ihren Patienten helfen, mit ihrem Asthma umzugehen, damit sie weiterhin ihren Lieblingsbeschäftigungen nachgehen können?

Achten Sie auf Ihre Patienten mit unkontrolliertem Asthma.
- Isabel litt an unkontrolliertem Asthma mit mehreren Exazerbationen pro Jahr, schlechter Inhalationstechnik und häufigen Nebenwirkungen.
- Leider ist Isabels Fall kein Einzelfall. Viele Asthmapatienten überschätzen ihre Symptomkontrolle und unterschätzen den Schweregrad ihrer Erkrankung, tolerieren Symptome und Einschränkungen in ihrer Lebensweise.1

Bestimmung der Faktoren, die zu einer schlechten Symptomkontrolle beitragen.
- Die Therapietreue bei der Asthma-Behandlung ist in der Regel mit etwa 30–50% gering, was zu einer schlechten Symptomkontrolle führen kann.2 In Isabels Fall waren ihre Angstzustände ein Hindernis dafür, dass sie ihre Symptome unter Kontrolle bringen konnte, und ihre Inhalationstechnik musste verbessert werden.
- Nach der Feststellung relevanter Komorbiditäten und vor der Änderung der Medikamentendosis bei einem Patienten sollte die Therapietreue überprüft werden. Die Inhalationstechnik sollte beurteilt und bei Bedarf sollte der Patient geschult werden.3

Bewerten, anpassen, überprüfen.
- Die Personalisierung von Isabels Asthmaversorgung war der Schlüssel zur Verbesserung ihrer Adhärenz, Inhalationstechnik und Symptomkontrolle.
- Nach der Bewertung der relevanten Komorbiditäten, Inhalationstechnik und Diagnose Ihrer Patienten ist es wichtig, ihre persönlichen Präferenzen und die gewünschten Behandlungsergebnisse zu ermitteln.4
- Regelmäßige Überprüfung der Symptome, Exazerbationen, Nebenwirkungen, Lungenfunktion und Patientenzufriedenheit.
HELFEN SIE, DAS ASTHMA-MANAGEMENT IHRER PATIENTEN MIT flutiform® pMDI ZU VERBESSERN5-8
Abkürzungen und Referenzen
pMDI, druckgasbetriebener Dosier-Inhalator.
1. Price D, et al. Prim Care Respir J. 2014;24:14009.
2. Bidwal M, et al. Res Social Adm Pharm. 2017;13(4):759–766.
3. Price D, et al. Respir Med. 2013;107(1):37–46.
4. Baggot C, et al. BMJ Open. 2020;10(8):e037491.
5. Usmani O S, et al. J Allerg Clin Immunol Prac. 2017;5(5):1378–87.
6. Schmidt O, et al. Respir Med. 2017;131:166–174.
7. Backer V, et al. Ther Adv Respir Dis. 2018;12:1–16.
8. Sicras-Mainar A, et al. BMJ Open. 2022;12(4):e053964.
®: flutiform® ist die eingetragene Marke der Jagotec AG, die unter Lizenz von Mundipharma verwendet wird.
®: Das „lung“-Logo ist die eingetragene Marke von Mundipharma.
Meldung von Nebenwirkungen
Nebenwirkungen können Sie dem Bundesinstitut für Arzneimittel und Medizinprodukte unter www.bfarm.de anzeigen oder per E-Mail an Mundipharma senden oder telefonisch melden.
Download Meldebogen (Zur Bearbeitung ist der Adobe Acrobat Reader notwendig.)
Telefon: 069506029000
Email: arzneimittelsicherheit@mundipharma.de
DE-FLU-2400002 | Datum der Vorbereitung: Oktober 2024
Biographie von Dr. Abel Pallarés Sanmartín:
Dr. Abel Pallarés Sanmartín ist Leiter der Abteilung für Pneumologie und Koordinator der Asthma-Abteilung am Universitätskrankenhaus von Ourense, Spanien. Bevor er diese Rolle übernahm, koordinierte er wichtige fachübergreifende Asthma-Abteilungen in Vigo und Pontevedra und sammelte 15 Jahre lang Erfahrung im Management von schwerem Asthma. Neben seiner medizinischen Praxis hat Dr. Abel Pallarés Sanmartín umfangreiche Forschungsarbeiten zum Thema Asthma-Management veröffentlicht und auf nationalen und internationalen Konferenzen Vorträge gehalten.